Метаболизм и метаболиты: что было раньше, курица или яйцо?
Если положить рядышком те факты, которые мы выяснили о метаболизме волосяного фолликула (ВФ), то получается вот что:
- стволовые клетки ВФ "практикуют" гликолиз для получения энергии, а получающийся на последней стадии гликолиза пируват преобразуется в лактат;
- интермедиаты гликолиза (глюкозо-6-фосфат) отправляются в пентозофосфатный путь, а получившиеся рибозо-5-фосфаты служат субстратом для синтеза нуклеотидов (и сохранения "стволовости");
- цикл Кребса в стволовых клетках немножечко как бы идет;
- в дифференцированных клетках основной метаболизм завязан на цикл Кребса.
Эти факты подтверждаются как морфологическими различиями в митохондриальном аппарате стволовых и дифференцированных клеток ВФ, так и в исследованиях активности митохондрий.
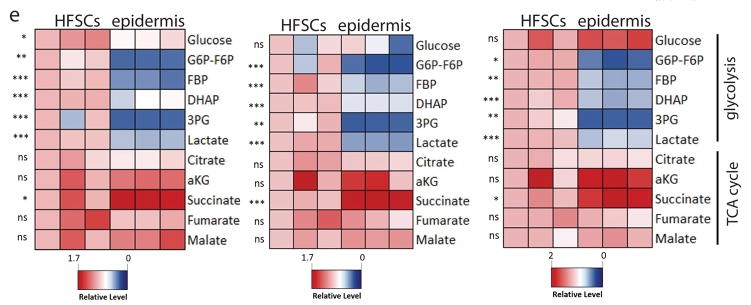
Кроме того, опубликованы количественные исследования метаболитов, подтверждающие эти факты. Например, группой исследователей [1] была проведена сравнительная оценка промежуточных метаболитов гликолиза и цикла Кребса в стволовых клетках ВФ и клетках эпидермиса. На приведенной картинке хорошо видны качественные различия (количественные данные концентраций метаболитов, к сожалению, не приведены в статье [1]). Мы видим, что:
- есть существенные различия в концентрации метаболитов гликолиза между стволовыми клетками ВФ и клетками эпидермиса;
- есть существенные различия в концентрации лактата;
- различия в концентрациях метаболитов гликолиза и цикла Кребса не слишком выражено в стволовых клетках ВФ и ярко выражено в клетках эпидермиса;
- концентрации сукцината и альфа-кетоглутарата выше в клетках эпидермиса, чем в стволовых клетках ВФ, однако и в стволовых клетках ВФ мы можем наблюдать относительное повышение концентраций некоторых интермедиатов цикла Кребса.
Это может говорить о следующем. В стволовых клетках гликолиз идет настолько активно, что концентрация его интермедиатов не успевает исчерпываться, а в клетках эпидермиса мы, наоборот, видим повышенную концентрацию интермедиатов цикла Кребса, что говорит об активности именно этого метаболического пути. Малая концентрация лактата в клетках эпидермиса подтверждает версию о том, что почти весь пируват отправляется в митохондрии и затем в ЦК. Однако чем объяснить наличие и лактата, и интермедиатов ЦК в стволовых клетках ВФ? Только ли тем, что в них имеет место и анаэробный путь, и аэробный?
в стволовых клетках действительно наблюдается повышенное потребление глюкозы, аналогичное эффекту Варбурга в раковых клетках (гликолиз - относительно дешевый способ получения энергии, но для него нужен НАД в окисленной форме. Превращение пирувата в лактат эффективно преобразует NADH обратно в NAD+, что обеспечивает бесперебойное прохождение гликолиза). В стволовых клетках интермедиаты гликолиза могут быть отправлены не только в пентозофосфатный путь (глюкозо-6-фосфат, G6P), но и на синтез аминокислот (3-фосфоглицерат, 3PG) и синтез липидов (дигидроацетонфосфат, DHAP) [1,2]
Возникают закономерные вопросы:
- Зачем стволовым клеткам лактат и куда он девается?
- Почему в стволовых клетках обнаруживается и лактат, и интермедиаты ЦК в сравнимых концентрациях?
- Как меняются концентрации ключевых метаболитов и что заставляет их меняться?
- Можно ли перепрограммировать клетку?
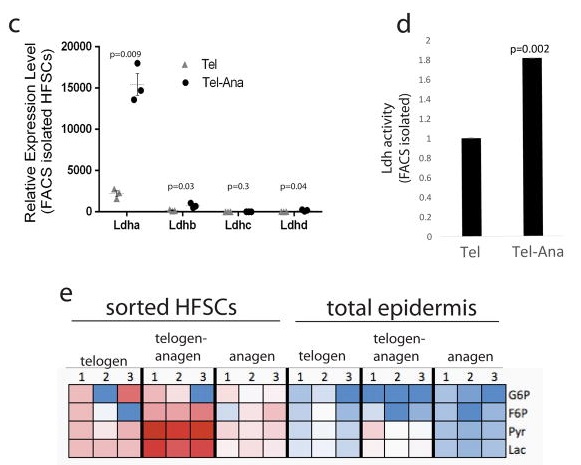
Тут выясняется интереснейшая вещь. Оказывается, при переходе из телогена в анаген в стволовых клетках резко возрастает активность лактатдегидрогеназы и, соответственно, подскакивает концентрация лактата. Затем в анагене активность данного фермента падает вместе с активностью гликолиза. Исследователи попытались выяснить, является ли повышение концентрации лактата всего лишь маркером перехода или же этот факт имеет прямое отношение к активации анагена. Для этого была выведена линия мышей с отключенной ЛДГ в фолликулах, и оказалось, что у этих мышей переход из телогена в анаген был нарушен. Однако привнесение дополнительного лактата (метод подробно описан в [1]) восстанавливало нарушенную функцию.
Разумеется, эта тема нуждается в дальнейших исследованиях. Насколько корректны полученные данные, насколько воспроизводимы результаты. Но если в самом деле окажется, что повышение концентрации лактата в стволовых клетках ВФ, готовых к дифференцировке, есть не только биохимический маркер перехода из телогена в анаген, если такое повышение в самом деле играет роль фактора активации процесса, то нам откроются интересные перспективы.
Получается, что в стволовых клетках по крайней мере часть пирувата преобразуется в лактат. Опять же мы знаем, что в стволовых клетках окислительное фосфорилирование приторможено, чтобы образующиеся активные окисленные субстанции (ROS, reactive oxygen species) не портили ДНК [6]. Этого можно добиться, перенаправляя входящий поток метаболитов в другое русло. Для цикла Кребса входной точкой служит ацетил-коА, который обычно получается из пирувата (может получиться и при окислении жирных кислот, но этот метаболический путь, как мы увидим потом, для стволовых клетках неактуален. Следовательно, остается только пируват). Если направить весь поток пирувата в лактатный путь (например, ингибированием пируватдегидрогеназного комплекса), то получим торможение цикла Кребса и вуаля - минимум активного окисления, минимальный поток бешеных электронов.
мы помним, что основная задача цикла Кребса - это создание потока электронов, перемещаемых на дыхательную цепь, с целью образования АТФ.
Налицо противоречие: с одной стороны, интермедиаты ЦК вполне себе есть. С другой стороны - никакого или минимум окислительного фосфорилирования, а в основном хардкор гликолиз. Как так?
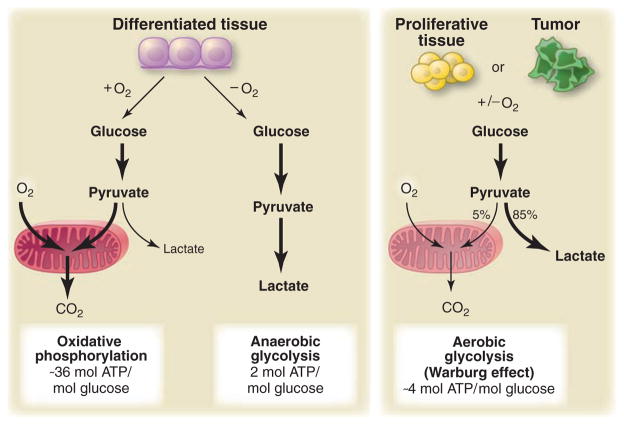
Наличие интермедиатов ЦК еще не означает, что идет полноценный цикл Кребса. Поясню мысль. В самом деле, митохондрии в стволовых клетках, прямо скажем, урезанные. Однако они все-таки есть. Значит, они делают что-то такое, что клетке обязательно нужно для поддержания гомеостаза.
Стволовые клетки, в том числе и стволовые клетки ВФ, в качестве основного типа метаболизма "практикуют" аэробный гликолиз, при котором примерно 15 процентов пирувата идет в митохондрии [10] (по данным [11] - в клетках ВФ распадается до CO2 примерно 10% поглощенной глюкозы). Это не только паллиативное решение для того, чтобы повысить выработку АТФ (на одну молекулу глюкозы приходится 36 молекул АТФ при полном окислительном фосфорилировании, либо 2 молекулы АТФ при анаэробном превращении в лактат и 4 молекулы - при аэробном гликолизе). Но митохондрии - это не только ценный мех цикл Кребса и окислительное фосфорилирование, это еще и три килограмма легкоусвояемого мяса митохондриальная ДНК и целый комплекс всяческих нужных ферментов. В них образуются метаболиты, которые затем отправляются в цитозоль для дальнейшей переработки там.
Номером один в этом списке необходимых интермедиатов будет наш старый знакомец Ацетил-КоА.
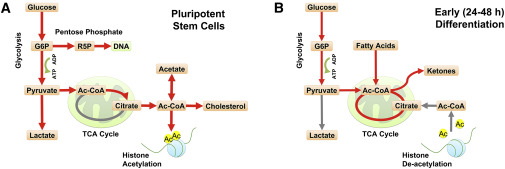
Оказывается, ацетил-коА жутко необходим стволовым клеткам для сохранения "стволовости". Как это происходит? Ацетил-коА служит донором ацетогрупп в реакциях ацетилирования гистонов [5]. Некоторая часть образовавшегося в результате гликолиза пирувата отправляется в митохондрии (для пирувата есть транспорт через мембраны [8]), где превращается в ацетил-коА путем окислительного декарбоксилирования при участии пируватдегидрогеназного комплекса и кофермента А. Дальше ацетил-коА, потеряв кофермент А и превратившись в цитрат (это происходит при участи другого митохондриального фермента - цитратсинтазы), в виде цитрата покидает митохондрии (для цитрата есть транспорт через мембраны [8]) и выходит в цитозоль. В цитозоле цитрат снова превращается в ацетил-коА (для этого необходим цитозольный оксалоацетат, который есть продукт окисления малата, и для этого необходим NAD+, а он уже есть - получился, когда пируват превращался в лактат).
Что произойдет, если запретить образование ацетил-коА из пирувата (например, с помощью фосфорилирования ПДГ соответствующей киназой [8])? Тогда весь пируват уйдет по лактатному пути. Соответственно нарушится процесс образования цитозольного ацетил-коА. Тогда ядро клетки не получит ацетогруппы. Кроме того, из-за пируват-лактатного превращения у нас образуется много NAD+, и он тоже должен куда-то деваться. Например, вот куда: высокая концентрация NAD+ активизирует SIRT1 деацетилазу гистонов [7,9], в результате клетка теряет "стволовость" и дифференцируется. Логично?
Это были всего лишь рассуждения. Но и на самом деле есть свидетельства, что такая метаболическая регуляция происходит в некоторых типах стволовых клеток, например, в стволовых клетках мышц [9]. Остается выяснить, а что происходит в стволовых клетках волосяных фолликулов?
Номером два в нашем списке интермедиатов будет альфа-кетоглутарат.
Оказывается, альфа-кетоглутарат служит кофактором в реакциях деметилирования гистонов и ДНК [7]. Но если цитрат покидает цикл Кребса, откуда берется альфа-кетоглутарат? А например так: глутамин, попавший в клетку, в цитозоле превращается в глутамат (при помощи глутаминазы). Глутамат отправляется в митохондрии (для переноса глутамата и аспартата через мембраны есть специальный транспорт). Глутамат в митохондриях преобразуется в альфа-кетоглутарат (для этого есть разные ферменты). По данным [11], глутамин поглощается волосяными фолликулами в значительном количестве (но необязательно стволовыми клетками, т.к. глутамин непосредственно участвует, например, в синтезе глутатиона, который в стволовых клетках как бы и не нужен, зато очень нужен в дифференцированных).
А на вопрос, куда девается из клетки лактат, ответ, скорее всего, будет таким: лактат из клетки выводится обычным образом и через печень вновь трансформируется в пируват. Возможно, при этом лактат играет еще роль какого-то переносчика сигналов, а может, и нет. В любом случае нужны дальнейшие исследования по этому вопросу.
Мы немножко попытались ответить на первые два вопроса, учитывая ту информацию, которая на сегодняшний день есть в открытом доступе. На два других вопроса попробуем ответить в следующей части, потому что они затрагивают такую очень новую область знаний о живой клетке, как метаболическое программирование.
Продолжение следует.
Литература:
-
Flores Aimee, Schell John, Krall Abby, Jelinek David, Miranda Matilde, Grigorian Melina, Braas Daniel, C White Andrew, Zhou Jessica, Graham Nick, Graeber Thomas, Seth Pankaj, Evseenko Denis, Coller Hilary, Rutter Jared, Christofk Heather, and E Lowry William
Lactate dehydrogenase activity drives hair follicle stem cell activation -
Ng Shyh-Chang and Huck-Hui Ng
The metabolic programming of stem cells -
Nobuaki Shiraki, Yasuko Shiraki, Tomonori Tsuyama, Fumiaki Obata, Masayuki Miura, Genta Nagae, Hiroyuki Aburatani, Kazuhiko Kume, Fumio Endo, Shoen Kume
Methionine Metabolism Regulates Maintenance and Differentiation of Human Pluripotent Stem Cells -
Биохимия витаминов
Е.Ф. Иваненко
Издательство "Вища школа", Киев, 1970 -
Arieh Moussaieff, Matthieu Rouleau, Daniel Kitsberg, Eran Meshorer, Daniel Aberdam, Yaakov Nahmias
Glycolysis-Mediated Changes in Acetyl-CoA and Histone Acetylation Control the Early Differentiation of Embryonic Stem Cells -
Shiwu Zhang, Chuanwei Yang, Zhenduo Yang, Dan Zhang, Xiaoping Ma, Gordon Mills, and Zesheng Liu
Homeostasis of redox status derived from glucose metabolic pathway could be the key to understanding the Warburg effect -
Ryan Janke, Anne E. Dodson, Jasper Rine
Metabolism and Epigenetics -
Federico Pietrocola, Lorenzo Galluzzi, José Manuel Bravo-San Pedro, Frank Madeo, Guido Kroemer
Acetyl Coenzyme A: A Central Metabolite and Second Messenger -
Tim S. Cliff, Stephen Dalton
METABOLIC SWITCHING AND CELL FATE DECISIONS: IMPLICATIONS FOR PLURIPOTENCY, REPROGRAMMING AND DEVELOPMENT -
Matthew G. Vander Heiden, Lewis C. Cantley, Craig B. Thompson
Understanding the Warburg Effect: The Metabolic Requirements of Cell Proliferation -
Williams R, Philpott MP, Kealey T.
Metabolism of freshly isolated human hair follicles capable of hair elongation: a glutaminolytic, aerobic glycolytic tissue.
